



 全国免费客服电话 0512-68566723
全国免费客服电话 0512-68566723 邮箱:sales@haipaixing.com
手机:15051551656
电话:0512-68566723
地址:苏州市高新区珠江路900号1号楼
发布时间:2021-02-07 人气: 190
标准、规范、方法不能被操作人员直接使用;
标准、规范、方法内容不便于理解;
标准、规范、方法规定不够简明或缺少足够的信息;
方法中有可选择的步骤,会在方法运用时造成因人而已,可能影响检测数据和结果正确性。
1、要素一:作业人员信任你的作业指导书
2、要素二:作业人员能快速理解作业指导书
3、要素三:作业指导书应该随时可以被作业人员拿到
4、要素四:作业指导书要与员工的培训保持一致
现场质量管理任重道远,制定一份好的SOP是重要的第一步。
参照GB/T 1.1《标准化工作导则,第1部分:标准的结构和编写规则》要求的格式,及检测方法文件化控制程序中规定包含的内容,将方法以增补SOP或内部检测方法的形式文件化,以保证检测人员正确使用和应用的一致性。
SOP的编写,必不可少的就是SOP的格式。一般来说,每个团队都会有一个固定的格式,来体现此份SOP是团队的所有物。比如说会写上哪个单位,哪个部门以及某个人在何年何月编写的SOP,一般都是插入页眉,写入这些信息。
明确SOP编写的主题是什么了。题目一定要清晰明确的体现这个主题,要让人一眼就明确题旨。比如说一份介绍仪器的操作,命名就可以直接为什么仪器的操作方法(步骤)。
既然SOP主要的目的是规范,那么文件内容一定要尽可能详尽,要把所有能想到的细节都囊括进去,只有这样,其他人才可能根据SOP做好事情。
SOP并不是圣典,它是可以变更的。如果现有的SOP不能满足现今的操作或者管理,那么就需要变更SOP了。
当然,无论是增加,销毁还是变更一份SOP,都要经过一系列固定的流程,SOP必须经审批、发布、归档、发放和使用等严格的流程,这些流程是赋予SOP公信力的方式,绝对不能省。最好还有专人负责SOP的管理,同时,SOP文件也要让公司所有员工都能看到,只有这样,才有助于管理。
最后,要让员工明白,所有的操作流程都要按照SOP进行,只有这样进行规范,SOP才能达到它的效用。
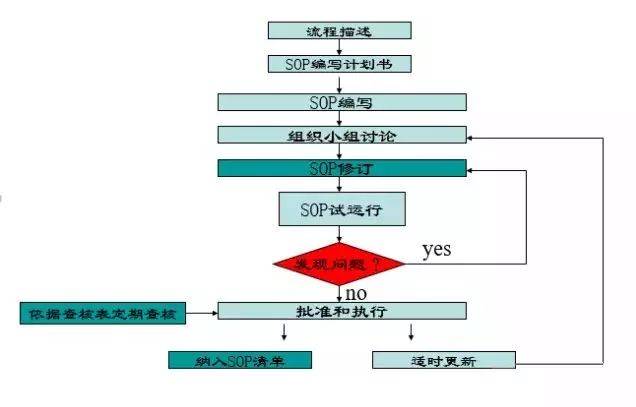
SOP编写计划书:明确SOP的编号、程序名称、编写人、初稿完成时间、小组讨论时间及最终的定稿时间。
SOP编写人员要求:操作好,有经验,有一定写作基础的一线员工沟通,打消编写人员的顾虑,并给予支持:专门的时间、提供相关资料等,编写小组要有团队精神。
SOP的讨论修订:统一认识,达成共识。SOP讨论会参与人员操作员、设备员(维修人员)、质量管理员、体系管理员、编写组负责人及1-2名与本岗位无关的人员讨论会,要做到互相挑战、各抒己见,必要时可进行现场确认。
SOP的试运行:目的:通过实践来检验SOP的合理性和可操作性。
SOP的定稿、批准和执行:建立与SOP相应的查核表(专业组长、质量管理员/内审员两级查核),定期查核CPCPR(CriticalProcess Control PointReview ):关键程序控制点回顾,关键步骤是对质量控制起重要、关键作用的步骤,通过建立关键步骤控制点并实施严格的质量控制,以提高作业质量的过程控制能力。
适时更新:当作业要求、设备状况等发生改变,一些操作方法的改进时,要对SOP进行评审和更新,定期回顾:确定回顾时间及参加人员,将回顾结果纳入更新内容将正式发布的SOP列入SOP清单。
SOP的编写要点:条理化、规范化、形象化、逻辑性正确性、精确性、可操作性,语句和结构条理清晰,文章前后有关联,指向分明。
作业步骤:操作步骤是SOP内容中的重点,必须简洁、明了,让人一看就懂,一看就知道怎么操作。SOP需要达到的效果是:一个新人一来就可以独立操作,且产品质量合格,这也是SOP的最高境界。
1) 标题:等同标准方法的标题或依据被检测的特性简化标题。
2) 范围:明确检测方法的浓度范围、样品基体和限制说明。
3) 检测的样品要求:包括特殊的采样要求、保存、样品制备或预处理等要求。
4) 方法原理:简单描述检测方法的原理。
5) 试剂与材料:所需的试剂和耗材的纯度与规格,以及试剂耗材质量核查方法等。所需的参考标准和标准物质。
6) 仪器和设备:包括仪器性能的要求。
7) 环境条件要求:温度、湿度、洁净度、供电以及电磁干扰等
8) 干扰:影响结果的干扰因素,包括谱线、化学、物理等干扰。
9) 分析步骤:详细的分析步骤描述。包括工作开始前所进行的检查;检查设备工作是否正常(需要时,在每次使用之前对设备进行校准和调整);质量控制测量的要求;观察和结果的记录方法。
10) 需要记录的数据以及分析和表达的方法。
11) 质量评估:接受(或拒绝)的准则和要求等。
12) 不确定度及评定不确定度的程序。
13) 安全措施:安全注意事项、与方法相关的风险告知等。
14) 参考文献
15) 检测原始记录表格式及检测报告格式
16) 授权批准:实验室负责人及质量负责人签发及日期;检测方法批准使用的日期等。
相关推荐